Lý thuyết: Biến thiên enthalpy trong các phản ứng hóa học
I. Phản ứng tỏa nhiệt, phản ứng thu nhiệt
- Phản ứng tỏa nhiệt là phản ứng giải phóng năng lượng dưới dạng nhiệt
- Phản ứng thu nhiệt là phản ứng hấp thụ năng lượng dưới dạng nhiệt
Ví dụ
- Phản ứng tỏa nhiệt: Đốt than, củi để không khí xung quanh ấm hơn

- Phản ứng thu nhiệt: Pha viên sủi vitamin C vào nước, thấy nước trong cốc mát hơn

II. Biến thiên enthalpy của phản ứng
1. Biến thiên enthalpy
- Khái niệm: Biến thiên enthalpy của phản ứng (nhiệt phản ứng) là nhiệt lượng tỏa ra hay thu vào của phản ứng ở điều kiện áp suất không đổi. Kí hiệu: ∆rH
- Phương trình hóa học kèm theo trạng thái của các chất và giá trị ∆rH gọi là phương trình nhiệt hóa học
Ví dụ: Phản ứng đốt cháy 2 mol khí hydrogen bằng 1 mol khí oxygen, tạo thành 2 mol nước ở trạng thái lỏng, tỏa ra nhiệt lượng 571,6 kJ.. Phản ứng trên có biến thiên enthalpy \({\Delta _r}H_{298}^o\) = -571,6 kJ, biểu diễn như sau:
2H2(g) + O2(g) → 2H2O(l) \({\Delta _r}H_{298}^o\) = -571,6 kJ
2. Biến thiên enthalpy chuẩn
- Khái niệm: Biến thiên enthalpy chuẩn là nhiệt tỏa ra hay thu vào của phản ứng được xác định ở điều kiện chuẩn: áp suất 1 bar (đối với chất khí), nồng độ 1 mol/L (đối với chất tan trong dung dịch) và nhiệt độ thường được chọn là 25oC (298 K), kí hiệu \({\Delta _r}H_{298}^o\)
3. Ý nghĩa của biến thiên enthalpy
∆rH > 0: phản ứng thu nhiệt
∆rH < 0: phản ứng tỏa nhiệt
- Giá trị tuyệt đối của biến thiên enthalpy càng lớn thì nhiệt lượng tỏa ra hay thu vào của phản ứng càng nhiều
Ví dụ: Xét 2 phản ứng
CH4(g) + 2O2(g) CO2(g) + 2H2O(l) \({\Delta _r}H_{298}^o\) = -890 kJ/mol
CH3OH(l) + 3/2 O2(g) CO2(g) + 2H2O(l) \({\Delta _r}H_{298}^o\) = -726 kJ/mol
=> Đốt 1 mol methane tỏa ra nhiệt lượng nhiều hơn đốt 1 mol methanol
- Các phản ứng xảy ra ở nhiệt độ phòng thường là phản ứng tỏa nhiệt, các phản ứng thu nhiệt thường xảy ra khi đun nóng
III. Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành
1. Khái niệm nhiệt tạo thành
- Nhiệt tạo thành (∆fH) của một chất là biến thiên enthalpy của phản ứng tạo thành 1 mol chất đó từ các đơn chất ở dạng bền vững nhất, ở 1 điều kiện xác định
- Nhiệt tạo thành chuẩn (\({\Delta _f}H_{298}^o\)) là nhiệt tạo thành ở điều kiện chuẩn
- Nhiệt tạo thành chuẩn của các đơn chất ở dạng bền vững nhất = 0. \({\Delta _f}H_{298}^o\)(O2(g)) = 0 kJ/mol
2. Tính biến thiên enthalpy của phản ứng theo nhiệt tạo thành
- Biến thiên enthalpy của phản ứng được xác định bằng hiệu số giữa tổng nhiệt tạo thành các chất sản phẩm (sp) và tổng nhiệt tạo thành của các chất đầu (cđ)
- Ở điều kiện chuẩn:
\({\Delta _r}H_{298}^o\) = \(\sum {{\Delta _f}H_{298}^o} (sp) - \sum {{\Delta _f}H_{298}^o} (c{\rm{d}})\)
- Lưu ý: Hệ số của các chất trong phương trình hóa học
Ví dụ: Xác định biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
4FeS2(s) + 11O2(g) → 2Fe2O3(s) + 8SO2(g)
biết nhiệt tạo thành \({\Delta _f}H_{298}^o\) của các chất FeS2(s), Fe2O3(s) và SO2(g) lần lượt là -177,9 kJ/mol, -825,5 kJ/mol và -296,8 kJ/mol
Lời giải:

IV. Tính biến thiên enthalpy của phản ứng theo năng lượng liên kết
- Phản ứng hóa học là quá trình phá vỡ các liên kết trong chất đầu và hình thành các liên kết mới để tạo thành sản phẩm
- Biến thiên enthalpy của phản ứng (mà các chất đều ở thể khí), bằng hiệu số giữa tổng năng lượng liên kết của các chất đầu và tổng năng lượng liên kết của các sản phẩm (ở cùng điều kiện nhiệt độ và áp suất)
- Ở điều kiện chuẩn
\({\Delta _r}H_{298}^o\) = \(\sum {{E_b}} (cd) - \sum {{E_b}} (sp)\)

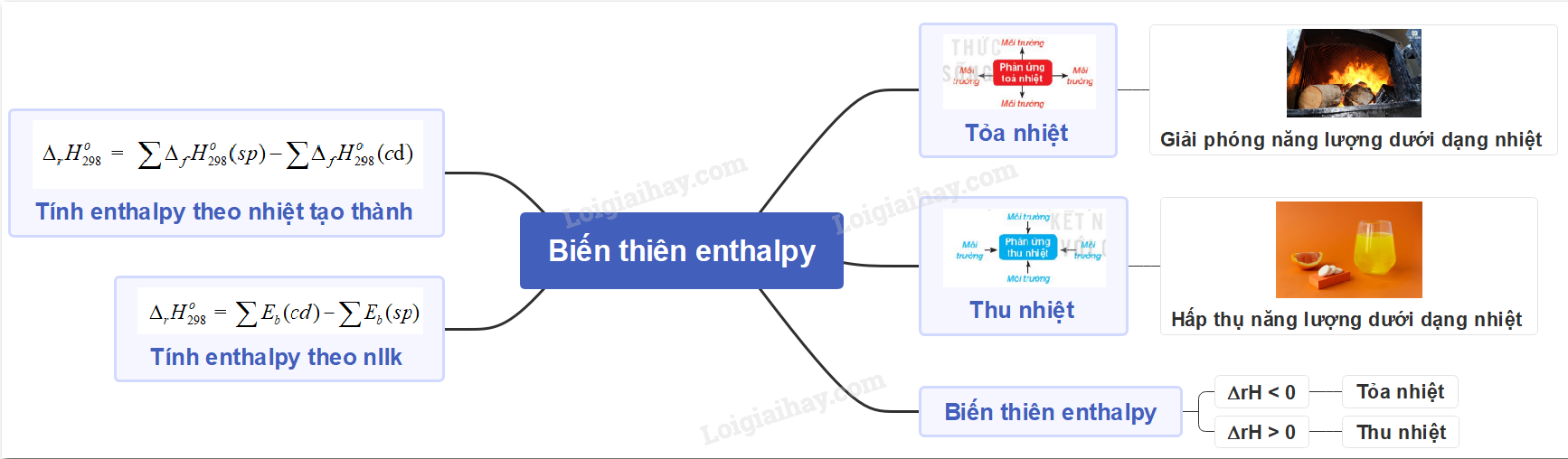
Sơ đồ tư duy: